Michal Dohányos, Jindřich Procházka, Kateřina Fliegerová*)
VŠCHT Praha, Ústav technologie vody a prostředí, *) ÚŽFG AVČR, Laboratoři anaerobní mikrobiologie.
Celková výroba „zelené“ elektrické energie z obnovitelných zdrojů se má v ČR podle národního indikativního cíle zvýšit ze 4,9 % v roce 2006 na 8 % v roce 2010. Z toho elektrická energie vyrobená z bioplynu činí v současné době cca 5 % a meziroční nárůst 9,3 % [1].
Anaerobní fermentace – biometanizace – tvorba bioplynu ze zbytkové, odpadové nebo cíleně pěstované biomasy je nejefektivnějším způsobem získávání energie z těchto materiálů. Tomu nasvědčuje i nárůst počtu nově stavěných bioplynových stanic. Dle ČIA bylo u nás k 1. prosinci 2008 celkem 113 BPS o souhrnném výkonu 50,32 MW a do roku 2015 se má zvýšit na 140 – 150 MWel. [1].
Hlavním substrátem pro zemědělské bioplynové stanice (BPS) je cíleně pěstovaná rostlinná biomasa. K pěstování rostlinné biomasy pro plynná biopaliva je k dispozici cca 9 % zemědělské půdy to představuje 390 tisíc ha [2].
Podle průběžného monitoringu bioplynových stanic již provozovaných nebo připravovaných k výstavbě, jejich naprostá většina předpokládá zpracovávání rostlinné biomasy jako nosného substrátu. Další suroviny jsou kejda resp. hnůj, vznikající při chovu hospodářských zvířat, odpady z potravinářského průmyslu a další jak uvádí následující přehled v tabulce 1.
Tabulka 1. Přehled potenciálních surovin pro BPS
| Druh odpadní biomasy | t/rok |
| Materiál živočišného původu (exkrementy, zpracování živočišných produktů. aj.) | 42 650 000 t/rok |
| Materiál rostlinného původu (rostlinné zbytky ze zemědělství, lihovarnické výpalky, pokrutiny, cukrovarnické řízky aj.) | 3 550 000 t/rok |
| Potravinářský průmysl (mláto, ostatní) | 370 000 t/rok |
| Ostatní průmysl (papíru a celulózy aj.) | 2000000 t/rok |
| Ostatní BRO (BRKO, zbytky ze stravoven aj.) | 2 850 000 t/rok |
| Kaly z ČOV | 300 000 t/rok. |
Zdroj: MZe, MPO, ČSŮ, CZ Biom
Rostlinná biomasa, kukuřičná a travní siláž, představuje přes 50 % hmotnostních všech substrátů. V přepočtu na obsah energie představuje rostlinná biomasa až 80 % energetického obsahu všech substrátů. Hlavním důvodem pro používání rostlinné biomasy k výrobě bioplynu je relativně vysoká produkce bioplynu z jednotky hmotnosti a zavedené agrotechnické postupy jejího pěstování, sklizně a konzervace. Anaerobní fermentací se získá z tuny kukuřičné siláže až 200 m3 bioplynu. Produkce bioplynu získaného anaerobní fermentací biomasy z trvalých travních porostů (TTP) je 150 – 190 m3/tunu travní siláže.
Jak vyplývá z výše uvedeného přehledu, velká část organických materiálů pro BPS je buď přímo rostlinného původu, nebo obsahuje zbytky rostlinné biomasy (např. kejda, zbytky potravin aj.).
Problémem bioplynových stanic zpracovávajících rostlinnou biomasu je především nízká účinnost procesu způsobená špatnou rozložitelností rostlinných materiálů. Nízká rozložitelnost se odráží v nižší produkci bioplynu, značná část organického uhlíku z rostlinných materiálů zůstává nevyužita (40 až 60 %). K potlačení této nevýhody je snaha prodlužovat dobu zdržení ve fermentorech, to vede k aplikaci velkoobjemových reaktorů s vysokými požadavky na energii, čímž nelze zajistit požadovanou ekonomičnost procesu.
Je všeobecně známo, že limitujícím faktorem při biologickém rozkladu rostlinné biomasy je její lignocelulózová struktura. Biologická rozložitelnost závisí mimo jiné také na poměru základních komponent rostlinné biomasy (celulóza, hemicelulóza, lignin).
Lignocelulózový komplex jako stavební materiál rostlin vzniká spojením několika paralelně uspořádaných celulózových řetězců stabilizovaných vodíkovými vazbami, přičemž pojivo mezi nimi vytvářejí další polysacharidy s větvenou strukturou, tzv. hemicelulózy. Hemicelulózy obsahují jako stavební jednotky různé monosacharidy (D-xylosu, D-galaktosu, L–arabinosu, D-glukosu a uronové kyseliny ). Matrici, v níž jsou uložena celulózová vlákna, tvoří kromě dalších (pektiny, extensin ) hlavně lignin.
Lignin je chemicky těžko definovatelná látka. Předpokládá se, že je to vysoce prokřížený větvený polymer vznikající dehydratací a polykondenzací. Je definován jako statistický polymer hydroxyfenylpropanových jednotek o relativní molekulové hmotnosti 10 000. Právě ligninová matrice stéricky brání celulolytickým extracelulárním enzymům v přístupu k celulózním vláknům a tudíž výrazně snižuje nejen rychlost, ale i celkový výtěžek hydrolýzy.
Zvýšení biologické rozložitelnosti a tím i výtěžnosti metanu lze dosáhnout vhodnou předúpravou suroviny. Všechny metody předúpravy jsou založeny na zpřístupnění složek materiálu enzymovému rozkladu. Zmenšením velikosti částic mechanickou nebo jinou dezintegrací dochází k podstatnému zvětšení povrchu a tím i k větší dostupnosti enzymovému rozkladu, u některých metod dochází i k hydrolýze makromolekulárních látek. V současné době je známo mnoho chemických a fyzikálně-chemických způsobů předúpravy, kdy je možno dosáhnout vyšší účinnosti převedení buďto ligninu nebo celulózy a hemicelulóz do kapalné fáze ve formě nízkopolymerních sloučenin, které jsou již snadno fermentovatelné. Vzhledem k tomu, že většina zpracovávaných organických látek je v partikulární formě, nejdůležitějším procesem rozkladu je jejich převedení do roztoku - hydrolýza. Ta probíhá v důsledku přítomnosti bakterií produkujících hydrolytické enzymy a její rychlost může být podstatně zvýšena různými způsoby dezintegrace a fyzikální nebo chemické předúpravy zpracovávaného materiálu [3].
Mechanické metody – sem patří různé způsoby dezintegrace tuhých složek substrátu – mletí, drcení apod. Zmenšením velikosti částic dochází ke zvětšení celkového povrchu a ke zlepšení přístupnosti organických látek v substrátu enzymatickému rozkladu.
Chemické metody – mezi chemické metody patří například působení alkálií, kyselin, nebo oxidačních činidel (např. ozon), které vede k destrukci složitých organických látek – hydrolýze Přídavkem chemikálií (např. H2SO4) se ale do systému mohou vnášet nežádoucí složky (síra).
Fyzikální metody – na příklad termická hydrolýza, ionizující záření, působení ultrazvuku. Dochází k destrukci složitých organických látek. Termická předúprava požadovaná u některých materiálů legislativou může být buď pasterizace při 70 °C nebo hygienizace při 130 °C podle druhu suroviny, obě metody vedle hygienizačního efektu fungují jako termická hydrolýza a zvyšují výtěžnost bioplynu.
Biotechnologické metody - enzymová nebo mikrobiální předúprava – použití čistých komerčně vyráběných enzymů – např. celuláz [4,7], přímé použití mikroorganizmů s vysokou celulázovou aktivitou - bachorové kultury [5,6], anaerobní houby [8].
Všechny tyto technologie jsou ekonomicky a technicky náročné a byly vyvinuty pro zpracování fytomasy na jiné produkty (high value products) a pro BPS se v provozním měřítku zatím nepoužívají. Tyto technologie většinou vyžadují vnos chemikálií a energie. V případě chemických nebo i termických metod produkt předúpravy často vykazuje toxické účinky na anaerobní biomasu.
Kromě mechanické dezintegrace a termické hydrolýzy, které se již v provozu sporadicky používají, jsou nejnadějnější biotechnologické metody zvýšení rozložitelnosti. Používání čistých enzymů (celuláz) je již komerční záležitostí, avšak je zde ještě mnoho nedořešených problémů. Výrobky různých producentů reagují různým způsobem, neexistuje jednoznačná metodika jejich aplikace, která by zaručovala výrobcem deklarované výkonnosti. Zatím nejsou prozkoumány závislosti funkce enzymových přípravků různých výrobců na změny technologických podmínek anaerobní fermentace.
Negativním faktorem je také vysoká cena enzymových přípravků a nutnost pravidelného dávkování do reaktoru.
Jednou z možností řešení je zvýšení rozložitelnosti rostlinné biomasy (lignocelulózových materiálů) a tím i zvýšení výtěžnosti bioplynu při anaerobní fermentaci těchto materiálů na bioplynových stanicích biotechnologickou metodou aplikace mikroorganizmů se zvýšenou celulázovou aktivitou (anaerobních hub) přímo do anaerobního reaktoru ve směsi s ostatními mikroorganizmy fermentace.
Anaerobní houby osidlují zažívací trakt býložravců, zejména přežvýkavců, a významným způsobem ovlivňují bachorový metabolismus. Tyto houby disponují celou řadu enzymů potřebných pro rozklad strukturních polysacharidů rostlinného krmiva. Produkují komplex enzymů pro štěpení celulózy (endoglukanázu, exoglukanázu a beta-glukosidázu) a hemicelulózy (xylanázu, xylosidázu, manázu, licheninázu a různé typy esteráz) [9]. Tyto hydrolázy umožňují houbám proniknout hluboko do rostlinného pletiva, odkrýt fermentační substráty nedostupné povrchově působícím bakteriím a kolonizovat a degradovat i vysoce odolná pletiva. Anaerobní houby, jako jediné houby vůbec, mají hydrolytické enzymy organizovány v organele zvané celulozom, která zajišťuje těmto houbám prioritní postavení mezi všemi celulolytickými mikroorganismy [10].
Komplexní působení celuláz a hemiceluláz navázaných v těchto „extracelulárních organelách“ je zodpovědné za mimořádnou degradační účinnost anaerobních hub, která převyšuje i komerčně užívané enzymatické preparáty vyráběné z aerobních hub rodu Trichoderma či Aspergilus [11]
Anaerobní houby potřebují pro své životní činnosti teplotu 35 až 40 °C, pH mírně alkalické a potřebují odstraňovat produkty své činnosti (vodík, CO2, mastné kyseliny aj. To předurčuje jejich symbiózu s metanogenními mikroorganizmy anaerobních reaktorů produkujících bioplyn. Výchozí hypotézou tohoto řešení je, že anaerobní houby svými enzymy rozruší strukturu rostlinné biomasy a tím uvolní další substráty pro anaerobní bakterie, které byly pro ně jinak nedostupné. To povede k celkovému zvýšení rozložitelnosti rostlinných materiálů a tím i ke zvýšení celkové produkce bioplynu. Zvýšení rychlosti rozkladu biomasy umožní také zkrátit dobu zdržení ve fermentoru a zvýšit celkovou výkonnost fermentoru.
Na ústavu technologie vody a prostředí VŠCHT byly provedeny předběžné pokusy, ve kterých byla sledována možnost uplatnění anaerobních hub v procesu produkce bioplynu. K pokusům byly použity kmeny anaerobní houby Anaeromyces mucronatus, izolované z bachorové tekutiny krávy v Laboratoři anaerobní mikrobiologie ÚŽFG AVČR, která se studiem anaerobních hub dlouhodobě zabývá.
Kultura Anaeromyces mucronatus je velmi dobře charakterizovaná a představuje stabilní kmeny vykazující dobrou celulolytickou i xylanázovou aktivitu [12,13]. Lze je dobře pěstovat v semisyntetických živných půdách a při jejich kultivaci dosahujeme dobré hmotnostní výtěžky, neboť vytvářejí husté větvené rhizomycelium.
Rod Anaeromyces byl popsán teprve v roce 1990 a patří k méně prostudovaným anaerobním houbám. Je to však jediný rod, u něhož byly pozorovány struktury připomínající spory, což vybavuje tento organismus schopností přežívat časově významná období bez běžně nutné subkultivace [14]. Tato vlastnost by mohla být výhodná pro zamýšlené pokusy.
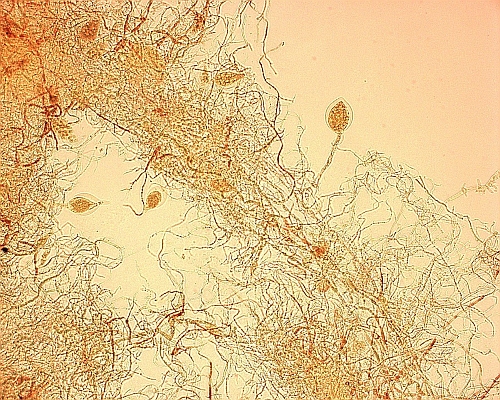
Obrázek 1: Snímek mycelia polycentrické houby Anaeromyces mucronatus KF4 ve světelném mikroskopu.
Bylo provedeno několik experimentů, ve kterých se porovnávala rozložitelnost travní siláže anaerobními houbami v různých podmínkách. Všechny experimenty proběhly v lahvích o objemu 600 ml, kde 400 ml tvořila kapalná fáze. Jako inokulum anaerobních bakterií byla použita fermentační směs z BPS Třeboň, která zpracovává vepřovou kejdu a malé množství čistírenských kalů. Jako substrát pak travní siláž. Charakteristiky fermentační směsi a substrátu jsou uvedeny v tabulce 1. Teplota, při které pokusy probíhaly, byla vždy 40 °C.
Tabulka 2 - Charakteristiky inokula a substrátu
| použití | sušina | org. sušina (% sušiny) | pH | |
|---|---|---|---|---|
| Tráva – (senáž) | substrát | 0,325 g/g | 94% | - |
| Třeboň kal | inokulum | 13,5 g/l | 60,50% | 7,7 |
Uspořádání a výsledky experimentu
Cílem experimentu bylo nepřímo ověřit možnosti růstu a funkce anaerobních hub v prostředí fermentační směsi a kvantifikovat jejich vliv na produkci bioplynu.
Byla porovnávána rozložitelnost travní siláže izoláty anaerobních hub v podmínkách fermentační směsi. V experimentu bylo zvoleno zatížení 3 g sušiny substrátu na litr fermentační směsi. Po nasazení a vytemperování byly přidány anaerobní houby a to v množství 5 ml suspenze kolonií v živném médiu, ve které byly kultivovány, do každé lahve (mimo testu bez přídavku hub – tam bylo přidáno pouze 5 ml vody). Houby byly přidány za dodržení anaerobních podmínek experimentu – injekční stříkačkou přes septum. Celkem bylo nasazeno do osmi lahví.
Po poklesu produkce bioplynu (28 den fermentace) byla do probíhajících testů přidána druhá dávka travní siláže a to 10 g čerstvé siláže do každé lahve. Třetí dávka - 5 g čerstvé siláže byla přidána po 50 dnech od přidání druhé dávky. Celkem ve třech dávkách bylo přidáno 19 g substrátu do každé lahve. Pokus dále probíhá čtvrtou dávkou.
Během experimentu bylo sledováno množství a kvalita produkovaného bioplynu a koncentrace NMK (nižších mastných kyselin). Naměřená kumulativní produkce bioplynu za celý průběh experimentu (tři postupné dávky substrátu) je uvedena na obrázku 2. Podrobné údaje o specifické produkci bioplynu v jednotlivých fázích pokusu – po jednotlivých přidáních substrátu uvádí tabulka 3. Jak vyplývá z průběhu experimentu, projevil se významný rozdíl mezi pokusy bez přídavku a s přídavkem hub. V pokusech s přídavkem hub byla produkce bioplynu vždy vyšší v průměru o 15 %. Složení bioplynu z jednotlivých pokusů bylo přibližně stejné, koncentrace metanu se pohybovala okolo 55 – 60 %.
V tomto příspěvku jsou prezentovány výsledky třech fází experimentu (tři přidání substrátu). V prvních dvou fázích všechny kmeny použitých anaerobních hub reagovaly přibližně stejně. Po třetím přidání (třetí fáze) v pokusech s kmeny KF4 a KF7 byl nárůst produkce bioplynu oproti kontrolnímu pokusu (bez hub) podstatně nižší – 0,36 % u KF4 a 3,27 % u KF7. Naproti tomu v pokusu s kmenem KF8 bylo zvýšení produkce BP 14,55% oproti kontrolnímu pokusu, tedy přibližně stejné zvýšení produkce bioplynu ve všech fázích experimentu.
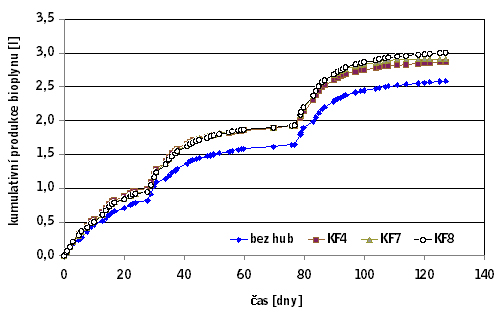
Obrázek 2. Kumulativní produkce bioplynu.
Tabulka 3. Specifická produkce bioplynu v jednotlivých fázích a za celou dobu experimentu.
| izolát | test | kumulativní produkce (ml) | specifická produkce na sušinu (ml/g) | specifická produkce na organickou sušinu substrátu (ml/g) | přínos hub v % oproti vzorku bez hub |
|---|---|---|---|---|---|
| bez hub | 1. | 812,50 | 454,09 | 513,91 | 0,00 |
| KF4 | 1. | 994,90 | 556,03 | 629,28 | 22,45 |
| KF7 | 1. | 956,50 | 534,57 | 604,99 | 17,72 |
| KF8 | 1. | 943,70 | 527,42 | 596,90 | 16,15 |
| bez hub | 2. | 833,90 | 242,35 | 257,82 | 0,00 |
| KF4 | 2. | 933,50 | 271,29 | 288,61 | 11,94 |
| KF7 | 2. | 977,10 | 283,96 | 302,09 | 17,17 |
| KF8 | 2. | 986,70 | 286,75 | 305,06 | 18,32 |
| bez hub | 3. | 946,90 | 550,00 | 585,50 | 0,00 |
| KF4 | 3. | 949,50 | 552,00 | 587,11 | 0,36 |
| KF7 | 3. | 977,50 | 568,00 | 604,42 | 3,27 |
| KF8 | 3. | 1082,90 | 630,00 | 669,60 | 14,55 |
| bez hub | celkem | 2593,30 | 393,14 | 420,39 | 0,00 |
| KF4 | celkem | 2877,90 | 455,63 | 467,40 | 15,89 |
| KF7 | celkem | 2911,10 | 452,76 | 473,70 | 15,16 |
| KF8 | celkem | 3013,30 | 457,20 | 489,10 | 16,29 |
Příčina snížení produkce u kmenů KF4 a KF7 po třetím přidání substrátu zatím není známá a je předmětem dalšího zkoumání. Kmen KF8 si zachoval svou aktivitu po třetím přidání substrátu, tj. po dobu cca 130 dní pokusu. Podrobné zdůvodnění bude pravděpodobně možné až v další fázi experimentů.
Závěr
Cílem tohoto příspěvku bylo ukázat směry výzkumu založené na využití nejnovějších poznatků anaerobní mikrobiologie zaměřené na možnosti intenzifikace produkce bioplynu.
V rámci tohoto projektu budou hledány izoláty anaerobních hub mající co nejvyšší celulázovou aktivitu a dobře „spolupracující“ s biomasou v anaerobním reaktoru.
Pro sledování skutečného zastoupení anaerobních hub v komplexní fermentační směsi se vyvíjí v Laboratořích anaerobní mikrobiologie ÚŽFG AVČR kvantifikační metoda. K tomuto účelu bude použita metoda „real-time PCR” kterou lze detekovat množství DNA.
Výzkum funkce anaerobních hub při anaerobní fermentaci rostlinných materiálů je zatím v začátcích, ale již první výsledky naznačují správný směr výzkumu a široké aplikační možnosti.
Literatura
[1] Gebauer P., (2007) Současnost a budoucnost OZE v ČR, konference: „Biomasa & Bioplyn“ Praha 27-28.11.2007, b.i.d. services s.r.o.
[2] Trnka J. (2007), Akční plán pro biomasu -úkoly pro období 2008 -2010, konference: „Biomasa & Bioplyn“ Praha 27-28.11.2007, b.i.d. services s.r.o.
[3] Dohányos M.: (2009). Zvyšování efektivity fermentace - nejnovější poznatky ve výzkumu a praxi. Biom.cz [online]. 2009-02-25 [cit. 2009-03-02]. Dostupné z WWW: http://biom.cz/cz/odborne-clanky/zvysovani-efektivity-fermentace-nejnovejsi-poznatky-ve-vyzkumu-a-praxi. ISSN: 1801-2655.
[4] Gerhardt, M., Pelenc, V., Bäuml, M. (2007). Application of hydrolytic enzymes in the agricultural biogas production: Results from practical applications in Germany. Biotechnology Journal, 2., 1481-1484.
[5] Barnes, S.P., Keller, J. (2003). Cellulosic waste degradation by rumen-enhanced anaerobic digestionWater Science and Technology Vol 48 No 4 pp 155–162.
[6] Gijzen, H. J., Zwart, K. B., Teunissen, M. J., Vogels, G. D. (1988) Anaerobic Digestion of Cellulose Fraction of Domestic Refuse by Means of Rumen Microorganisms. Biotechnology and Bioengineering, Vol. 32, Pp. 749-755.
[7] Zhang, Y.H.P., Lyn, L.R. (2004). Toward an Aggregated Understanding of Enzymatic Hydrolysis of Cellulose: Noncomplexed Cellulase Systems Biotechnology and Bioengineering ,Vol. 88, No. 7, 797-824.
[8] Hodrová, B., Kopečný, J., Káš, J. (1998). Cellulolytic enzymes of rumen anaerobic fungi Orpinomyces joyonii and Caecomyces communis., Res. Microbiol. 149, 417-427.
[9] Ljungdahl LG. (2008). The cellulase/hemicellulase system of the anaerobic fungus Orpinomyces PC-2 and aspects of its applied use. Ann. N.Y. Acad. Sci. 1125, 308-321.
[10] Doi RH. (2008). Cellulases of mesophilic microorganisms – cellulosome and noncellulosome producers. Ann. N.Y. Acad. Sci. 1125, 267-279.
[11] Dijkerman R, Bhansing DCP, Op den Camp HJM, van der Drift C, Vogels GD. (1997). Degradation of structural polysaccharides by the plant cell-wall degrading enzyme system from anaerobic fungi: an application study. Enzyme Microbial Technol. 21, 130-136.
[12] Fliegerová K, Mrázek J, Voigt K. (2006). Differentiation of anaerobic polycentric fungi by rDNA PCR-RFLP. Folia Microbiol 51, 273-277.
[13] Fliegerová K, Pažoutová s, Mrázek J, Kopečný J. (2002). Special properties of polycentric anaerobic fungus Anaeromyces mucronatus. Acta vet. 71, 441-444.
[14] Brookman JL, Ozkose E, Rogers S, Trinci APJ, Theodoru MK. (2000). Identification of spores in the polycentric anaerobic gut fungi which enhance their ability to survive. FEMS Microbiol. Ecol. 31, 261-267.
Tento příspěvek byl vytvořen v rámci řešení projektu VaV MŽP ČR č. SP/3g4/129/07 "Intenzifikace produkce bioplynu".
Předneseno na konferenci „BIOPLYN 2009“, Gas s.r.o, 8-9. dubna 2009, České Budějovice,
Autor: Michal Dohányos