Anaerobní rozklad čistých organických látek je z hlediska převodu hmoty a energie ze substrátu do produktů dobře znám a definován; v praxi se však málokdy setkáváme se substrátem s přesně definovaným složením, většinou je nutné anaerobně zpracovávat komplexní substrát, navíc s proměnlivým počtem i poměrem jeho složek. Při provádění bilance anaerobního mikrobiálního systému s komplexním substrátem je třeba postihnout nejen stechiometrické, ale i energetické vztahy mezi substrátem a produkty.
Pro popis kvality substrátu z hlediska jeho energetického obsahu je používáno několik kritérií. K tomuto účelu může sloužit ekvivalent dostupných elektronů obsažených v substrátu [l]. Jako dostupné elektrony se označují ty, které mohou být přeneseny na kyslík při spálení látky. Na znalosti biochemických reakcí tvorby ATP je založen výpočet množství ATP v molech syntetizovaných při rozkladu jednoho molu substrátu [2]. Další možnost zjištění energetické účinnosti procesu je porovnání spalných tepel substrátu a produktů [3,4].
Účinnost produkce aerobní biomasy vzhledem k vynaložené katabolické energii lze charakterizovat růstovým výtěžkem odvozeným ze spotřeby kyslíku na rozklad substrátu. Množství kyslíku potřebné pro oxidaci komplexního substrátu lze odhadnout na základě stanovení chemické spotřeby kyslíku (CHSK). V anaerobním systému, kde jsou jiné finální akceptory elektronů než kyslík, lze použít vztah ekvivalentu dostupných elektronů a jednoho molu kyslíku a používat pro míru energetického obsahu substrátu kyslíkové jednotky ve formě CHSK (nebo TSK, TSK je teoretická spotřeba kyslíku na úplnou oxidaci dané organické látky vypočítaná z elementárního složení).
Pro celkovou hmotově energetickou bilanci anaerobního procesu používají někteří autoři [5] elementární složení substrátu. Stejné jako u dříve uvedených kritérií není tento údaj vždy snadno dostupný. Stanovení CHSK proti tomu je jednou z nejčastěji prováděných analýz ve vodohospodářských i dalších laboratořích, používá se pro návrh, řízení i kontrolu technologie procesu a u většiny hodnocených substrátů bývá tento údaj k dispozici.
Uvažujeme organickou sloučeninu sumárního vzorce CxHyOz, kde indexy x, y, z značí počet atomů jednotlivých prvků. Úplná oxidace této látky probíhá podle rovnice:
CxHyOz, + nO → x CO2 + y/2 H20 (1)
kde
n = 2x + y/2 – z (2)
Číslo n udává počet atomů kyslíku potřebných k úplné oxidaci dané organické látky (teoretickou spotřebu kyslíku). Protože jeden atom kyslíku představuje dva elektronové ekvivalenty, číslo 2n udává elektronový ekvivalent molekuly dané organické látky, tj. počet elektronů, které tato molekula předá při úplné oxidaci finálnímu akceptoru elektronů.
Obecná stechiometrická rovnice vzniku metanu podle Buswella [6] je následující:
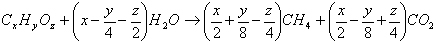 (3)
(3)
Množství vzniklého metanu závisí na počtu volných elektronů, které má molekula dané organické látky k dispozici. Jednoduchým způsobem lze dokázat, že k úplné oxidaci metanu vzniklého reakcí (3) spotřebujeme stejné množství kyslíku jako k oxidaci původní látky (l):
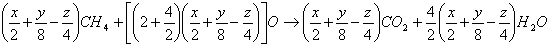
po úpravě:
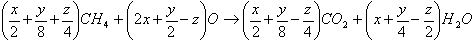 (4)
(4)
Součet rovnic (4) a (3) dává rovnici (l).
Z výše uvedeného vyplývá, že při metanizaci veškerá energetická zásoba výchozí látky (neuvažujeme-li i spotřebu energie k růstu) zůstává zachována ve vzniklém metanu.
Poměr počtu ekvivalentních elektronů 2n k počtu atomů uhlíku v molekule organické látky udává ,,stupeň redukovatelnosti" dané látky - γ.
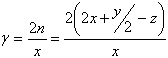 (5)
(5)
γ lze stanovit také z hmotově energetické bilance substrátu a ze znalosti jeho elementárního složení [5].
Vychází se z toho, že v oxidoredukčních reakcích jsou C, H, P a Fe donorem 4, l, 5 a 3 volných elektronů a prvky O, N a S jsou akceptory 2, 3 a 2 volných elektronů. Bilance elektronů substrátu obecného složení CxHyOz je daná vztahem 4x + 1y - 2z, což vztaženo na jeden atom uhlíku představuje ,,stupeň redukovatelnosti" substrátu γ = 4 + y/z - 2 z/x.
Číslo γ je měřítkem teoretické spotřeby kyslíku (vyjádřeno v počtu atomů kyslíku potřebných na oxidaci 1 molu organické látky) na jeden atom uhlíku. V hmotnostním vyjádření vztah (5) přechází na tvar:
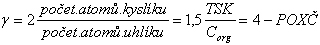 (6)
(6)
(POXČ—průměrné oxidační číslo atomu uhlíku)
Provedená hmotnostně energetická bilance prokázala,že bilance metanizačního procesu může být prováděna v kyslíkových jednotkách (TSK, CHSK), vztahy (l) až (5) lze použít k výpočtu teoreticko výtěžnosti metanu a složení bioplynu.
Výtěžnost metanu závisí na druhu substrátu, zejména na jeho oxidačním stupni, tj. na množství dostupných elektronů, které má molekula substrátu k dispozici. Tyto veličiny jsou definovány jako POXČ (průměrné oxidační číslo atomu uhlíku, udávající stupeň oxidace uhlíkového atomu v molekule) nebo jako γ (stupeň redukovatelnosti substrátu). Čím je nižší POXČ nebo čím je vyšší γ, tím je výtěžnost metanu vyšší. Mezní hodnoty dosahují sloučeniny CO2 a CH4,
| POXČ | γ | |
| CO2 | + 4 | 0 |
| CH4 | - 4 | 8 |
Bilance výtěžnosti metanu pro některé definované substráty je uvedena v tabulce 1. Ze vztahů (l) až (4) vyplývá, že hodnota TSK vzniklého metanu je rovna TSK původní látky. Když nahradíme TSK experimentálně stanovenou hodnotou CHSK, bude maximální teoretická výtěžnost metanu:
CHSKsubstrátu = CHSKmetanu (7)
Skutečná výtěžnost metanu je nižší, protože:
Přesnější je bilance odstraněné CHSK:
CHSKodstr = CHSKmetanu + CHSKbiomasy (8)
kde
CHSKodrtr. — skutečně odstraněná (tj. biologicky rozložená) část substrátu v průběhu metanizace,
CHSKmetanu — množství vzniklého metanu vyjádřeno v CHSK,
CHSKbiomasy — představuje část substrátu spotřebovanou na růst a krytí energetických nároků biomaay.
Ze vztahu (8) můžeme na základě provedeného pokusu stanovit produkci biomasy.
Maximální teoretickou výtěžnost metanu vyjádřenou jako hmotnostní množství metanu na hmotnostní jednotku přivedeného substrátu YCH4teor spočítáme ze stanovené CHSK nebo vypočítané TSK podle vztahu:
YCH4teor. = 0,25 CHSK [g/g] (CH4, substrát) (9)
Pro rychlejší přepočet metanu a CHSK jsou uvedeny v tabulce 2 přepočtové koeficienty.
Tabulka 2. Přepočtové koeficienty mezi CH4 a CHSK
| 1 mol CH4 |
2 mol O2 64 g CHSK 22,4 l *) |
| 1 g CHSK |
0,25 g CH4 0,35 l CH4 *) |
| 1 g CH4 |
4 g CHSK 1,4 l *) |
| 1 l CH4 | 2,857 g CHSK |
*) Pozn.: Platí za standardních podmínek, teplota 0°C, tlak 101,3 kPa
Bilance CHSK při tvorbě metanu je patrna ze schématu na obrázku 1.
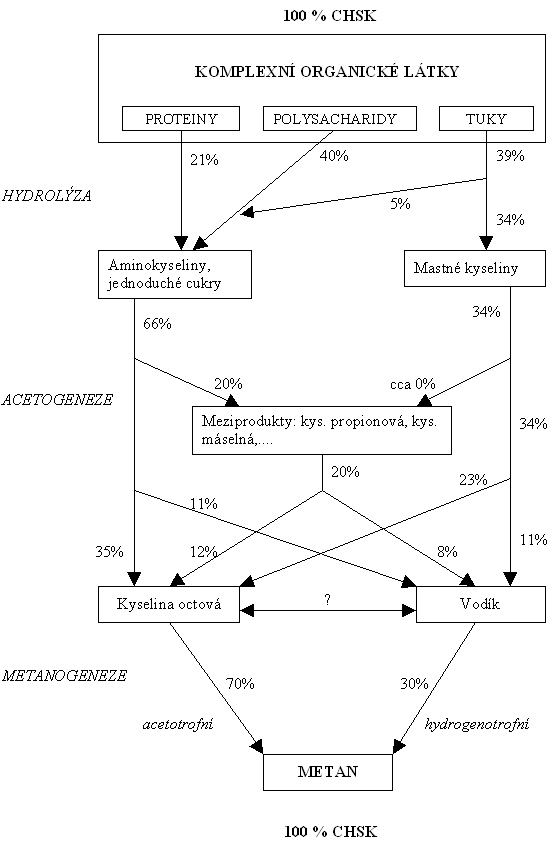
Obr.1. Bilance CHSK v průběhu tvorby metanu anaerobním rozkladem komplexních organických látek – čistírenský kal (zpracováno dle [10], [11]).
Ze vztahu (3) vyplývá, že z jedné molekuly obecného organického substrátu o sumárním vzorci CxHyOz, vzniká (x/2 + y/8 — z/4) CH4,. Vztažením na l atom uhlíku dostáváme:
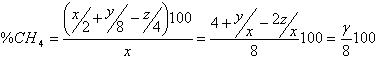 (10)
(10)
Dosazením vztahu (6) dostáváme výraz pro výpočet teoretické koncentrace metanu na základě stanovení CHSK substrátu a množství organického uhlíku substrátu:
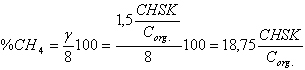 (11)
(11)
nebo při znalosti POXČ substrátu:
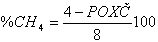 (12)
(12)
Při výpočtu skutečné koncentrace metanu v bioplynu je nutno provést korekci na CO2 rozpuštěný nebo vázaný v kapalné fázi fermentační směsi (HCO3-). Jeho množství závisí na fyzikálně chemických a technologických podmínkách v reaktoru. Rozpustnost metanu ve vodě je zanedbatelná.
Jak již bylo uvedeno, výtěžnost metanu závisí na množství dostupných elektronů v molekule substrátu. V případě přítomnosti dalších prvků v molekule substrátu (např. dusíku a síry), které v oxidoredukčních reakcích jsou akceptory volných elektronů, dochází ke snížení množství volných elektronů pro tvorbu metanu a tím ke snížení výtěžnosti metanu. Takto působí zejména dusík a síra a jejich sloučeniny, které se často vyskytují jako složky substrátu pro metanizaci. Míra ovlivnění výtěžnosti metanu závisí na oxidačním stupni daného prvku.
Dusík se vyskytuje jako organicky vázaný (většinou amino skupiny nebo heterocykly) a dále ve formě NH4+, NO2- a NO3-. Amoniakální dusík jakožto sloučenina s nejnižším oxidačním stupněm dusíku elektronovou bilanci neovlivňuje.
Organicky vázaný dusík ve velké většině případů vystupuje jako akceptor tří volných elektronů a při oxidaci (při stanovení CHSK) přechází na NH3, takže podíl dusíku je již zahrnut v TSK nebo CHSK substrátu a je možno použít k výpočtu výtěžku metanu vztah (9), viz např. aminokyseliny, leucin, lysin — viz tabulka 1.
Kyslíkaté sloučeniny dusíku N2- a NO3- které jsou často přítomny v některých průmyslových odpadních vodách, v anaerobním prostředí podléhají redukci na N2, čímž snižují množství volných elektronů substrátu.
Spotřeba energetického substrátu pro redukci NO2- a NO3- je následující [8]:
NO2-:
C6H12O6 + 8 NO2- → 4 N2 + 4 HCO3- + 2 CO32- + 4 H2O (13)
1 NO2- → 3 e- → ¾ O2 (14)
1 g NO2-—N → 1,714 g O2 (CHSK) (15)
NO3-:
5 C6H12O6 + 24 NO3- → 12 N2 + 24 HCO3- + 6 CO2 + 18 H2O (16)
1 NO3- → 5 e-→ 5/4 O2 (17)
1 g NO3-—N → 2,86 g O2 (CHSK) (18)
Při stanovení CHSK dusičnany hodnotu CHSK neovlivňují. Dusitany jsou oxidovány na dusičnany. Na l g NO2—N se spotřebuje 1,143 g O2, o tuto hodnotu se zvýší stanovená CHSK substrátu.
Pro korekci výtěžnosti metanizace na dusičnany a dusitany musíme od stanovené CHSK substrátu odečíst CHSK potřebnou k redukci NO2- a NO3- (rovnice 13, 14, 15, 16, 17, 18).
Výtěžnost metanu korigovaná na obsah NO2- a NO3- bude následující:
YCH4teor = 0,25 (CHSK-N) [g/g], (CH4, substrát) (19)
kde N je korekce CHSK na obsah NO2—N a NO3—N:
N = 2,86 (NO2-N + NO3-N) [g] (O2, CHSK).
Síra se vyskytuje organicky vázaná v aminokyselinách ve formě S2-, v sulfoskupinách (S4+) nebo v anorganických sloučeninách jako SO42-, SO32-.
Při stanovení CHSK se síra v nižších oxidačních stupních oxiduje na SO3.
Redukce síranů probíhá podle rovnice:
C6H12O6 + 3 SO42- → 3 S2- + 6 CO2 + 6 H2O (20)
1 SO42- → 8 e- → 4/2 O2, (21)
1 g SO4—S → 2 g O2 (CHSK) (22)
(nebo l g SO42- → 0,67 g O2)
Korekce výtěžnosti metanu na obsah síry se provede tak, že od celkové CHSK substrátu se odečte kyslíkový ekvivalent síry.
YCH4teor = 0,25 (CHSK - S) [g/g] (CH4, substrát) (23)
kde S je korekce CHSK na obsah síry:
S = 2 x (celkový obsah síry) [g] (O2, CHSK).
Sumární rovnici oxidace obecného substrátu s obsahem N a S možno psát:
CxHyOzNpSq + [2x + (y-3p)/2 - z + 3q] O → xCO2 + (y-3p)/2 H2O + p NH3 + q SO3 (24)
Bilance metanizace v kyslíkových jednotkách umožňuje na základě stanovení CHSK substrátu dobrý odhad produkce metanu. A také umožňuje výpočet produkce anaerobní biomasy. Pro různé substráty se koeficient produkce biomasy pohybuje v rozmezí 0,04—0,25 g/g (odstraněná CHSK, sušina vzniklé biomasy).
Stanovením CHSK a obsahu organického uhlíku substrátu (obě metody jsou dostupné ve vodohospodářských laboratořích) je možno stanovit teoretickou koncentraci metanu v bioplynu.
Vztah mezi teoretickou a skutečnou výtěžností metanu je dán druhem substrátu a také podmínkami procesu metanizace. Pro dobře probíhající proces metanizace byly pro některé čisté substráty stanoveny následující poměry teoretické a skutečno výtěžnosti metanu (tabulka 3).
Tabulka 3. Teoretické a skutečné výtěžnosti metanu pro některé čisté substráty (podle [5])
| substrát | YCH4skutečný / YCH4teor |
| kyselina octová | 0,97 |
| metanol | 0,98 |
| glukóza | 0,99 |
| fenol | 0,9 – 0,94 |
Příklad kyslíkové bilance procesu metanizace je možno uvést z údajů publikovaných Wangem a kol. [9], kteří popisují anaerobní čištění modelové odpadní vody obsahující fenol jako jediný zdroj uhlíku v laboratorním anaerobním reaktoru s expandovaným ložem. Bilance je uvedena v tabulce 4.
Teoretická produkce metanu uvedená v tabulce 4 byla vypočtena podle rovnice (9), teoretická koncentrace metanu podle rovnice (11) a odhad produkce biomasy podle vztahu (8). Z tabulky vyplývá, že teoretická produkce metanu je vyšší o 8 až 12 % (podle zatížení) než skutečná produkce naměřená experimentálně. Rozdíl mezi experimentální a teoretickou produkcí CH4 je způsoben v tomto případě neúplnou konverzí substrátu (účinnost čistění) a spotřebou na růst biomasy.
Produkce metanu vztažená na odstraněnou CHSK je nižší než experimentálně zjištěná produkce o ca 4 až 9 %. Tento rozdíl je způsoben tím, že část CHSK substrátu (4—9 %) je využita k růstu a ke krytí energetických požadavků biomasy. Z výsledků lze tedy odhadnout produkci biomasy za daných podmínek na 4—9 % z odstraněné CHSK (Y = 0,04—0,09).
Skutečný obsah metanu v bioplynu je podstatně vyšší než teoreticky vypočítaný (ca o 9—18 %). Je to způsobeno tím, že teoretický obsah metanu nebyl korigován na rozpustnost CO2 v kapalné fázi.
Tabulka 4. Bilance produkce metanu (zpracováno podle [9]
| R I | R II | R III | |
| Zatížení [kg/m3 d] (CHSK) | 2,00 | 3,62 | 7,20 |
| CHSK [g/d] | 13,00 | 23,53 | 46,80 |
| Corg. [g/l] | 0,58 | 1,21 | 2,28 |
| Fenol [g/l] | 0,70 | 1,49 | 2,36 |
| Účinnost odstranění CHSK [%] | 97,50 | 97,00 | 91,80 |
| Teoretická produkce CH4 (Yteor) [l/d] | 4,55 | 8,23 | 16,38 |
| Teoretická produkce CH4 v CHSK [g/d] | 13,00 | 23,51 | 46,80 |
| Teoretický obsah CH4 v bioplynu [%] | 64,60 | 56,00 | 59,10 |
| Teoretická produkce CH4 vypočítaná z odstraněné CHSK (YCHSKodstr) [l/d] | 4,44 | 7,98 | 15,04 |
| Specifická teoretická produkce CH4 vypočítaná na přivedenou CHSK [l/g d] | 0,34 | 0,34 | 0,32 |
| Teoretická produkce CH4 vypočítaná z odstraněné CHSK vyjádřena v CHSK [g/d] | 12,67 | 22,81 | 42,96 |
| Skutečná produkce CH4 (experimentální, Yexp) [l/d] | 4,02 | 7,57 | 14,78 |
| Skutečná produkce CH4, experimentální v CHSK [g/d] | 11,49 | 21,63 | 42,23 |
| Specifická produkce CH4, experimentální na přivedenou CHSK, [l/g d] | 0,31 | 0,32 | 0,32 |
| Skutečný obsah CH4 v bioplynu [%] | 82,40 | 74,40 | 68,10 |
| Nerozložená CHSK [g/d] | 0,33 | 0,72 | 3,84 |
| Produkce biomasy v CHSK [g/d] | 1,19 | 1,18 | 0,73 |
| Produkce biomasy v % CHSKodstr [%] | 9,38 | 5,17 | 1,71 |
[l] Mayberry, W. R. — Précházka, G. J. — Payne, W. J.: Growth yields of bacteria on selected organic compounds. J. Appl. Microbiol., 15, 1967. 1332—1338.
[2] Bauchop, T. — Elsden, S. R.: The growth of microorganisms in relation to their energy supply. J. Gen. Microbiol., 23. 1960, 457—969.
[3] Nagai, S.: Mass and energy balances for microbial growth kinetics. Adv. Biochem. Eng. 11, 1979, 49—83.
[4] Minkevič. I. G. — Jerošin, V. K.: Productivity and heat generation of ferrnenfcation under oxygen limitation. Folia Microbiol., 18, 1973, 376 až 387.
[5] Sobotka. M. et al.: The mass-energy balance of anaerobic methano producfcion. Folia Microbiol., 1983, 28, 195—204.
[6] Symons, G. E. — Buswell. A. M.: The methane fermentation of carbohydraces. J. Am. Chein. Soc., 55, 1933, 2028—2029.
[7] Gujer, W. — Zehnder, A. J. B.: Conversion proccss in anaerobic digestion. Wat. Sci. Tech. 15, 1983, 127—167.
[8] Grau, P. — Wanner, J.: Kyslíková bilance nitrifikačně denitrifikačního procesu. Vodní hospodářství, B 10, 1986, 265—270.
[9] Wang, Y. T. at al.: Anaerobic treatment of phenol by an expanded-bed reactor. Journal WPCF, 58, 1986, 227—233.
[10] Mata-Alvarez, J.: Biomethanization of the organic fraction of municipal solid waste. IWA Publishing, London, (2003), ISBN: 1900222140
[11] Siegris,t H., Renggli, D., Gujer, W.: Mathematical modelling of anaerobic mesophilic treatment. Wat. Sci. Tech. 27 (2), 25-36, (1993).
Tabulka 1. Bilance výtěžnosti metanu pro některé substráty
| Substrát | Reakce | TSK [g/g] | Corg [g/g] | γ | POXČ | YCH4teor [l /g] | Teret. obsah CH4 [%] |
| šťavelová kyselina | 4 C2H2O4 → CH4 +7 CO2 | 0,178 | 0,270 | 1,00 | 3,00 | 0,062 | 12,5 |
| mravenčí kyselina | 4 CH2O2 → CH4 +3 CO2 | 0,347 | 0,261 | 2,00 | 2,00 | 0,121 | 25,0 |
| octová kyselina | C2H4O2 → CH4 + CO2 | 1,067 | 0,400 | 4,00 | 0,00 | 0,373 | 50,0 |
| glukóza | C6H12O6 → 3 CH4 + 3 CO2 | 1,067 | 0,400 | 4,00 | 0,00 | 0,373 | 50,0 |
| fenol | 2 C6H6O → 8 H2O + 7 CH4 + 5 CO2 | 2,380 | 0,765 | 4,66 | -0,66 | 0,833 | 58,3 |
| máselná kyselina | 2 C4H6O2 + 2 H2O→ 5 CH4 + 3 CO2 | 1,817 | 0,546 | 5.00 | -1,00 | 0,636 | 62,5 |
| kapronová kyselina | C6H12O2 + 2 H2O → 4 CH4 + 2 CO2 | 2,205 | 0,619 | 5,34 | -1,34 | 0,772 | 66,6 |
| palmitová kyselina | 2 C16H22O2 + 14 H2O → 23 CH4 + 9 CO2 | 2,871 | 0,750 | 5,74 | -1,74 | 1,005 | 71,8 |
| butanol | C4H10O + H2O → 3 CH4 + CO2 | 2,595 | 0,649 | 6,00 | -2,00 | 0,908 | 75,0 |
| metanol | 4 CH4O → 3 CH4 + CO2 + 2 H2O | 1,498 | 0,375 | 6,00 | -2,00 | 0,524 | 75,0 |
| leucin | 4 C6H13O2N + 10 H2O → 15 CH4 + 9 CO2 + 4 NH3 | 1,832 | 0,550 | 5,00 | -1,00 | 0,641 | 62,5 |
| lysin | 2 C6H14O2N2 + 6 H2O → 7 CH4 + 5 CO2 + 4 NH3 | 1,534 | 0,493 | 4,67 | -0,67 | 0,537 | 58,3 |
Autor: Michal Dohányos